Chemisches Gleichgewicht Spickzettel
Chemisches Gleichgewicht Spickzettel
Bisher haben wir gelernt, dass Reaktionen in eine Richtung stattfinden. Aber jetzt beschäftigen wir uns mit reversiblen Reaktionen. Die unten angegebene Reaktion findet in einem geschlossenen Behälter statt.
A(g) + B(g) → C(g) + D(g)
Zu Beginn reagiert A mit B und erzeugt C und D Gas. Dies ist eine Vorwärtsreaktion, und die Geschwindigkeit dieser Reaktion wird wie folgt geschrieben:
Reaktionsgeschwindigkeit = kf. [A]. [B]
Da die Konzentrationen von A und B mit der Zeit abnehmen, nimmt auch die Vorwärtsreaktionsrate ab. Darüber hinaus kollidieren produzierte C und D Moleküle miteinander und bilden A- und B-Moleküle. Dies nennt man Umkehrreaktion, und die Geschwindigkeit wird wie folgt geschrieben:
Reaktionsgeschwindigkeit = kr. [C]. [D]
Die Gleichgewichtskonstante der folgenden Reaktion wird geschrieben als;
aA + bB ↔ cC + dD
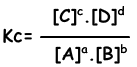
Homogenes und heterogenes Gleichgewicht
Wenn sich alle in der Gleichgewichtsreaktion befindlichen Stoffe in einer Phase befinden, handelt es sich um ein homogenes Gleichgewicht. Wenn mindestens einer der Stoffe eine andere Phase aufweist, handelt es sich um ein heterogenes Gleichgewicht. Wenn wir die Gleichgewichtsgleichung eines heterogenen Gleichgewichts schreiben, schreiben wir in die Gleichgewichtsgleichung keine reinen Feststoffe und keine reinen Flüssigkeiten.
CaCO3(s) ↔ CaO(s) + CO2(g)
Diese Reaktion ist eine heterogene Gleichgewichtsreaktion und wir schreiben CaCO3(s) und CaO (s) nicht in die Gleichgewichtsgleichung.
Gleichgewichtskonstante in Bezug auf Partialdruck
Gaskonzentrationen sind direkt proportional zum Partialdruck von ihnen. Somit können wir eine Gleichgewichtskonstante in Form von Partialdrücken schreiben.
N2(g) + 3H2(g) ↔ 2NH3(g)
Die Gleichgewichtskonstante dieser Reaktion in Bezug auf die Konzentrationen ist;
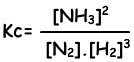
Die Gleichgewichtskonstante dieser Reaktion in Bezug auf den Partialdruck ist;
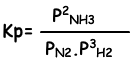
Faktoren, die das chemische Gleichgewicht beeinflussen
1. Einfluss der Konzentration auf das Gleichgewicht: Hinzufügen oder Entfernen von Substanzen in das Gleichgewicht des Reaktionseffekts. Zum Beispiel erhöhen die Zugabe von Reaktanten oder das Entfernen von Produkten die Produktausbeute. Im Gegensatz dazu erhöhen die Zugabe von Produkten oder die Entfernung von Reaktanten die Ausbeute an Reaktanten. Mit anderen Worten, in der ersten Situation verschiebt sich das Gleichgewicht nach rechts und in der zweiten Situation verschiebt sich das Gleichgewicht nach links.
2. Einfluss der Temperatur auf das Gleichgewicht:
- In einer endothermen Reaktion; Erhöhen der Temperaturverschiebung nach rechts und Erhöhen der Gleichgewichtskonstante.
- In einer endothermen Reaktion; Erhöhen des Temperaturverschiebungsgleichgewichts nach links und Verringern der Gleichgewichtskonstante.
3. Einfluss des Drucks auf das Gleichgewicht:
- Wenn eines der im Behälter befindlichen Stoffe bei konstanter Temperatur und konstantem Druck entfernt oder hinzugefügt wird, ändert sich der Druck des Systems. Eine Änderung der Konzentration wird jedoch nicht als Druck berücksichtigt.
- Die Temperatur kann bei konstantem Volumen geändert werden. Selbst wenn sich der Druck ändert, berücksichtigen wir in dieser Situation Änderungen der Temperatur, während wir eine Gleichgewichtskonstante finden.
- Wenn sich bei Gasreaktionen die Molzahl nicht ändert, wirkt sich der Druck nicht auf das Gleichgewicht aus.