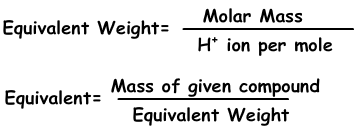Concentración con ejemplos
Concentración
La concentración es la cantidad de soluto en la solución dada. Podemos expresar la concentración de diferentes maneras como la concentración por ciento o por los topos.
1) Concentración por porcentaje:
Es la cantidad de soluto se disuelve en 100 g de disolvente. Si la concentración de la solución es de 20%, entendemos que hay 20 g de soluto en 100 g de solución.
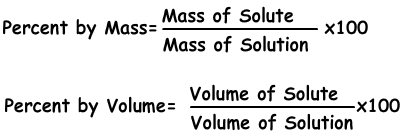
Ejemplo: 10 g de sal y 70 g de agua se mezclan y la solución preparada. Buscar concentración de la solución en masa por ciento.
Solución:
La masa de soluto: 10 g
Masa de la solución: 10 + 70 = 80 g
80 g de solución incluye 10 g de soluto
100 g de solución incluye X g de soluto
¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯
X = 12,5 g%
O utilizando la fórmula;
Por ciento de la masa = 10.100/80 = 12,5%
Ejemplo: Si la concentración en masa de 600 g de NaCl es de 40%, encontramos cantidad de soluto en masa en esta solución.
Solución:
100 g de solución con 40 g de soluto
600 g de solución incluye X g de soluto
¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯
X = 240 g de sal NaCl se disuelve en una solución.
Ejemplo: Si añadimos 68 g de azúcar y 272 g de agua a la solución de 160 g con una concentración del 20%, encontramos una concentración final de esta solución.
Solución:
Masa de la solución es de 160 g de azúcar antes de la adición y el agua.
100 g de solución incluye 20 g de azúcar
160 g de solución incluye X g de azúcar
¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯
X = 32 g de azúcar
La masa de soluto después de la adición = 32 + 68 = 100 g de azúcar
Masa de la solución después de añadir =272 +68 + 160=500 g
500 g de solución incluye 100 g de azúcar
100 g solución incluye X g de azúcar
¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯
X = 20% es la concentración de la solución final.
2) La concentración en moles:
Podemos expresar la concentración de soluciones por los topos. Número de moles por litro que se llama molaridad se muestra con M.
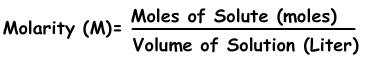
Ejemplo: El uso de 16 g de NaOH, 200 ml de solución se prepara. ¿Cuáles de las siguientes afirmaciones son verdaderas para esta solución? (Masa molar del NaOH es 40 g)
I. La concentración de la solución es 2 molar
II. Volumen de agua en la solución es de 200 ml
III. Si añadimos agua a la solución, moles de soluto disminuye.
Solución: Moles de NaOH
I. nNaOH=16/40=0,4 mole
V=200 mL= 0,2 Litros
Molaridad = 0,4 / 0,2 = 2 molar
I es verdad
II. Dado que el volumen de la solución es de 200 ml, el volumen de agua es menor de 200 ml. II es falso.
III. Si añadimos agua a la solución, el volumen de la solución aumenta, sino moles de soluto no cambia.
Ejemplo: 4,4 g de sal XCl2 se disuelve en 100 ml de agua y forma 0,4 molar XCl2 solución. Encontrar la masa molar de X. (Cl = 35)
Solución:
Molaridad = n / V
n = M.V donde V = 100 ml = 0,1 L y M = 0,4 molar
n = 0,1.0,4 = 0,04 mol
Si 0,04 moles XCl2 es 4,4 g
1 mol XCl2 es? g
¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯
? = 110 g XCl2
La masa molar de XCl2 = X 2. (35) = 110
X = 40 g / mol
3) La molalidad:
La molalidad es la otra expresión de la concentración de las soluciones. Se denota con “m” y la fórmula de la molalidad es;
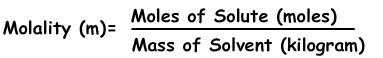
4) La normalidad:
Podemos expresar la concentración de otra manera con normalidad utilizando los equivalentes de solutos.

Equivalentes se pueden definir como: número de moles de iones H+ en ácidos y OH- ion en las reacciones de base. Por ejemplo, 1 mol de H2SO4 da 2 iones H+, el equivalente de H2SO4 2. Nos encontramos con un peso equivalente;