Propiedades de las disoluciones y los cálculos de solución
Propiedades de las disoluciones
Punto de ebullición, punto de congelación, presión de vapor, y propiedades como la densidad de las soluciones son diferentes de las propiedades del disolvente puro. Por ejemplo, el agua hierve a 100 oC, en la sal hierve contra una solución de agua por encima de 100 oC.
Si la materia disuelta en el agua no es volátil, que impiden la evaporación del agua y como un punto de ebullición del resultado de los aumentos de agua y punto de congelación del agua disminuye. En invierno, la sal se vierte en el camino para disminuir el punto de congelación del agua.
En una solución, el aumento de temperatura de ebullición es directamente proporcional a la concentración molar de las partículas en la solución.
En soluciones líquidas, la disminución de puntos de congelación y la presión de vapor es inversamente proporcional a la concentración molar de las partículas en la solución.
La conductividad de la electricidad es directamente proporcional a la concentración molar de los iones en las soluciones. Por ejemplo, el alcohol y el azúcar no conducen la electricidad.
Ejemplo: Hay la misma cantidad de agua en los tanques siguientes. Si disolvemos siguientes solutos en estos tanques, encontrar relación entre la conductividad eléctrica de estas soluciones.
I. 1 mol NaCl
II. 2 mol azúcar
III. 1 mol Al(NO3)3

Solución:
La conductividad eléctrica de soluciones depende de la concentración de iones molar de la solución. Ahora nos encontramos con la concentración de iones de soluciones en cada tanque.
I. NaCl(s) → Na+(aq) + Cl-(aq)
1 mol 1 mol 1 mol
Hay dos iones de un lunar en la primera solución.
II. Puesto que el azúcar se solvatación molecular, no hay de iones en la solución. Por lo tanto, no conduce la electricidad.
III. Al(NO3)3(s) → Al+3 + 3NO3-1
1 mol 1 mol 3 mol
Hay 4 moles de iones en la solución.
Los volúmenes de las soluciones son iguales entre sí relación entre lo que otros la conductividad eléctrica de soluciones se convierte;
III> I> II
Los cálculos solución
Ejemplo: Si nos preparamos tres soluciones en 1 atm de presión con 1 L de agua y NaCl 0,1 mol, 0,2 mol de NaCl, 0,3 mol de NaCl para cada solución, compare el punto de ebullición, punto de congelación y presiones de vapor de estas soluciones.

Solución:
NaCl (s) → Na + (aq) + Cl-(aq)
1 mol NaCl da un mol de Na + y Cl-1 mol total de 2 iones mol.
En el primer contenedor, 0,1 NaCl 0,2 mol de iones da
En segundo contenedor, 0,2 NaCl da 0,4 mol de iones
En tercer recipiente; NaCl 0,3 mol de iones da 0,6
Puntos de ebullición de soluciones relacionadas con la cantidad de soluto en la solución. El aumento en la cantidad de soluto punto de aumentar la ebullición de la solución. Relación entre puntos de ebullición de la solución;
III> II> I
Si el punto de ebullición de la solución es alta, entonces la presión de vapor de la misma es baja. Así relación entre las presiones de vapor de soluciones se convierte;
I> II> III
Si el punto de ebullición de la solución es alta, entonces el punto de congelación de la misma es baja. Así relación entre los puntos de congelación de las soluciones se convierte;
I> II> III
Ejemplo: Comparar los puntos de ebullición de las siguientes soluciones;
I. insaturados X sólida solución de agua
II. Saturadas X sólida solución de agua
III. Sobresaturada X sólida solución de agua
Solución:
Como la cantidad de soluto en la solución aumenta, también aumenta la temperatura de ebullición. Por lo tanto, III cuenta con la mayor soluto en él entonces II y finalmente se convierte en relación I. entre ellos;
III> II> I
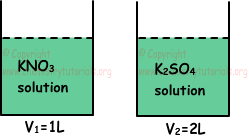
Ejemplo: Los contenedores se indican a continuación incluye soluciones bajo la misma temperatura y presión. Si la concentración molar de iones K + en los dos recipientes son iguales, ¿cuáles de las siguientes afirmaciones son verdaderas para estas soluciones?
I. Número de moles de soluto asuntos son iguales.
II. Presión de vapor del primer contenedor es superior a segundo recipiente.
III. Punto de ebullición de la primera solución es menor que la segunda solución.
Solución:
Supongamos que, la concentración molar de [K+]=2 M;
I.
1 mol de KNO3 incluye un mol K+, por lo que 2 M de iones K+ proviene de 2 M de KNO3 .
1 mol K2SO4 incluye 2 mol K+, por lo que 2 M de iones K+ proviene de una M K2SO4. Por lo tanto, moles de KNO3 y K2SO4 disueltos;
nKNO3=V1.M1=1.2=2 mol
nK2SO4=V2.M2=2.1=2 mol
Por lo tanto, el número de moles de materia disuelta son iguales, que es verdad.
II. 2 M KNO3 ofrece 4 M de iones y un K2SO4 M da 3 M de iones. Presión de vapor es inversamente proporcional a la concentración molar de las partículas en la solución. Por lo tanto, la presión de vapor del segundo envase es más alto que el primer contenedor. II es falso.
III. Punto de ebullición es directamente proporcional a la concentración molar de las partículas en la solución, por lo tanto la solución en un recipiente primer punto de ebullición más alto que la solución en el segundo recipiente. III es falsa.