Atoom Structuur Examen 2 En Probleem Oplossingen
Atoom Structuur Examen 2 En Probleem Oplossingen
1. Welke van de volgende relaties over 714X-3 ion zijn waar?
I. p+=n0
II. e->p+
III. Massagetal =p+ + e-
Oplossing:
Atoomnummer = aantal protonen =7 p+=7
Massa nummer=p+ + n0
14=7+n0
n0=7
n0=p+=7 I is waar
We vinden lading van ionen als;
lading van ionen=p+ - e- -3=7-e-
e-=10 (e->p+) II is waar
Massa nummer is 14 daarentegen, som van p+ en e- is 17
III is fout.
2. Positief geladen ionen worden kation genoemd en negatief geladen ionen worden anion genoemd. De onderstaande tabel toont het aantal elektronen en protonen van gegeven elementen.

Welke van de hierboven gegeven elementen zijn kation?
Oplossing:
In een neutraal atoom is het aantal protonen gelijk aan het aantal elektronen.
Aantal protonen van X is groter dan aantal elektronen, dus X is kation.
Aantal protonen van Y is gelijk aan aantal elektronen, dus Y is neutraal.
Aantal protonen van Z is groter dan aantal elektronen, dus Z is kation.
3. Als het aantal elektronen van X+3, Y-3 en Z gelijk zijn, welke van de volgende beweringen waar zijn voor hen.
I. X heeft de grootste nucleaire lading
II. Volume van Y-3 ion is groter dan anderen
III. Aantrekking van één elektron; X+3> Z > Y-3
Oplossing:
Laat me het aantal elektronen met “a” tonen. Lading van ion kan worden gevonden met de volgende vergelijking;
opladen = p+-e-
Voor X+3 ion;
+3 = p + -a dan, p + = a + 3 en a+3X+3
Voor Y-3 ion;
-3 = p + -a dan, p + = a-3 en a-3Y-3
Voor Z atoom; p+=e- dan p+=a en aZ0
Lading van kern is gelijk aan aantal protonen. X heeft dus de grootste nucleaire lading. I is waar.
Omdat ze een gelijk aantal elektronen hebben, is de aantrekking van één elektron recht evenredig met het aantal protonen. Als het aantal protonen dan toeneemt, neemt ook de aantrekking van elektronen toe. Zo wordt relatie; X+3 > Z > Y-3 III is waar
Volume is omgekeerd evenredig met aantrekking van één elektron.
X+3 < Z < Y-3II is waar
4. Cu heeft twee isotopen; 63Cu in 70% en 65Cl in 30%. Vind de gemiddelde atoommassa van Cu-atoom.
Oplossing: We gebruiken de volgende formule om de gemiddelde atoommassa van Cu te vinden;
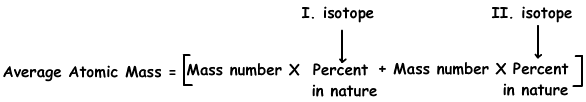
Gemiddelde atoommassa van Cu=63.(70/100) + 65.(30/100)
Gemiddelde atoommassa van Cu=63,6 g
5. Zoek een atoomnummer van een element met een elektronenconfiguratie die 6p2 duurt.
Oplossing: Om het atoomnummer van het element te vinden, moeten we alle orbitalen schrijven tot 6p2 en het totale aantal elektronen.
1s22s22p63s23p64s23d104p65s24d105p66s24f145d106p2
Sum of number of electrons is 82. So it also has 82 protons and atomic number is 82.
6. Zoek het aantal gevulde en half gevulde orbitalen van 14Si element.
Oplossing: We schrijven eerst de elektronenconfiguratie van 14Si en tonen vervolgens elektronen in orbitalen.
14Si: 1s22s22p63s23p2
Orbitalen;
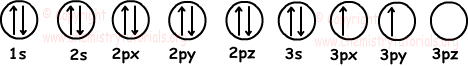
Zoals u kunt zien in het gegeven diagram, heeft 14Si 6 gevulde en 2 half gevulde orbitalen.