Atoom Structuur Examen 3 En Probleem Oplossingen
Atoom Structuur Examen 3 En Probleem Oplossingen
1 . Is er sferische symmetrie in 6C atoom?
Oplossing:
Elektronenconfiguratie van C; C: 1s22s22p2
Omdat orbitaal 2 elektronen bevat, is er geen sferische symmetrie in dit element. Om sferische symmetrie te hebben, moeten elementen gevulde of halfgevulde orbitalen hebben.
2. Witte fosfor en rode fosfor zijn allotroop van fosforelement. Welke van de volgende uitspraken zijn waar voor hen;
I. Elektronenstructuren van atomen daarvan zijn verschillend
II. Ze hebben verschillende dichtheden
III. Chemische eigenschappen van verbinding P2O5 gevormd door deze allotroop zijn verschillend.
Oplossing:
I. Allotrope omvat atomen behoren tot hetzelfde element. Aldus moeten elektronenstructuren van atomen hetzelfde zijn. I is waar.
II. Omdat allotrope verschillende fysische eigenschappen hebben, moeten dichtheden ervan verschillend zijn. II is waar.
III. Chemische eigenschappen van allotrope met andere elementen zijn hetzelfde. III is fout.
3. Welke van de volgende paren hebben dezelfde chemische eigenschappen?
(11H, 12D)
I. 2656Fe+2 en 2656Fe+3
II. 2656Fe en 2756Co
III. H2O en D2O
Oplossing:
Om dezelfde chemische eigenschappen te hebben, moeten zaken hetzelfde aantal protonen en elektronen hebben.
I. Aangezien ze een gelijk aantal protonen hebben, maar een verschillend aantal elektronen, zijn hun chemische eigenschappen verschillend.
II. Zowel aantal protonen als neutronen zijn verschillend. Dus de chemische eigenschappen ervan zijn ook verschillend.
III. Ze hebben hetzelfde aantal protonen en elektronen. Ze hebben dezelfde chemische eigenschappen.
4. Welke van de volgende beweringen zijn onjuist voor X en Y atomen?
X: 1s22s22p63s1
Y: 1s22s22p63s23p64s1
I. Y is opgewonden toestand van X
II. X en Y zijn atomen van hetzelfde element
III. Y is stabieler dan X
Oplossing:
I. Elektronenconfiguratie van X wordt geschreven volgens de grondtoestand van het atoom. Maar in Y wordt één elektron van 3s geschreven naar 4s orbitaal. Dus is Y de opgewonden toestand van X. Als energie aan X wordt gegeven, kan het in Y veranderen. I is waar.
II. Omdat ze allebei 11 elektronen hebben, horen ze bij hetzelfde element. II is waar.
III. Omdat energie van X kleiner is dan energie van Y, is deze stabieler dan Y. III is fout.
5. Als het aantal gevulde orbitalen van X 7 is en de half gevulde orbitalen 2 is, welke van de volgende kunnen dan worden gevonden?
I. Atoomnummer
II. Aantal valentie-elektronen
III. Massagetal
Oplossing:
We tekenen 7 gevulde en 2 half gevulde orbitalen zoals; 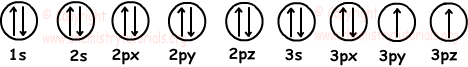
Elektronen configuratie :
1s22s22p63s23p4
Aantal elektronen: 2 + 2 + 6 + 2 + 4 = 16
In neutraal atoom is het aantal elektronen gelijk aan het aantal protonen en het atoomnummer. Met behulp van gegeven gegevens kunnen we dus het atoomnummer van het element vinden. We kunnen ook valentie-elektronen van elementen vinden door ze toe te voegen.
3p en 3s zijn valentie-orbitalen.
Aantal valentie-elektronen = 2 + 4 = 6
We moeten het aantal neutronen weten om het massagetal te vinden. Van gegeven gegevens kunnen we geen massanummer vinden.
6. Welke van de volgende uitspraken is waar voor 17X, 20Y en 18Z elementen?
I. Y- en X-elementen vormen YX2 verbinding
II. Y en Z+1 ion zijn iso-elektronisch
III. Elektronenconfiguratie van Z+1 als laatste met 4s2 orbitaal.
Oplossing:
17X heeft elektronenconfiguratie: 1s22s22p63s23p5
20Y heeft elektronenconfiguratie: 1s22s22p63s23p64s2
X accepteert één elektron en Y geeft twee elektronen om een nobele gaselektronenconfiguratie te hebben. X is niet-metaal en Y is metaal, ze vormen de volgende verbinding;
YX2 I is waar
Aangezien de elektronenconfiguratie van Y en Z+1 verschillend zijn, zijn ze noch iso-elektronisch. II is fout.
Z+1 heeft elektronenconfiguratie: 1s22s22p63s23p5
III is fout.